郭俊红医生的科普号
- 精选 揭秘诊断金标准病理诊断肺结节之浸润性腺癌
 郭俊红 主治医师 上海市肺科医院 病理科851人已观看
郭俊红 主治医师 上海市肺科医院 病理科851人已观看 - 精选 病理医生为什么诊断了原位腺癌?
 郭俊红 主治医师 上海市肺科医院 病理科777人已观看
郭俊红 主治医师 上海市肺科医院 病理科777人已观看 - 精选 I期肺腺癌复发的高危因素
I期(早期)肺腺癌复发的高危因素有哪些?快速了解病理报告中的危险信号!社会经济及网络迅速发展,大家对健康的关注持续升高,从各个取到获取的信息量也不断攀升,近几年,大家没有像以前那样“谈癌色变”了,因为很多早期癌症通过手术是可以治愈的,但是有些手术完全切除后的早期癌症也有复发的风险,接下来我们来聊一聊早期肺腺癌复发的高危因素到底有哪些?病理报告中哪些术语需要提高警惕?首先要了解几个概念:何为I期(早期)肺癌?没有肺门淋巴结转移的肺癌通常称为临床早期肺癌,但是,临床认为是早期肺癌的患者经手术后病理证实并非都是“早期”肺癌。术后病理根据2021版胸部肿瘤WHO分类-肺癌TNM分期,简言之肿瘤大小≤4cm并且没有淋巴结转移的肺癌为I期(早期)肺癌。何为肺腺癌?通常我们所说的肺腺癌指的是浸润性肺腺癌,是指具有腺样分化、产生粘液或表达肺泡细胞标记的恶性上皮细胞性肿瘤。肺腺癌的亚型包括贴壁型,腺管型,乳头型,微乳头型及实性型。变异型腺癌包括浸润性粘液腺癌、胶样腺癌、胎儿型腺癌和肠型腺癌。划重点 肺腺癌复发的高危因素到底有哪些?1.容易复发的腺癌亚型:腺癌中的高级别结构。1)微乳头型,微乳头型是肺腺癌中最险恶的类型。经典型微乳头由缺乏纤维血管轴心的瘤细胞簇构成。微乳头概念扩展-丝状型微乳头,是肿瘤细胞生长在纤细、花边状、无纤维血管轴心的细长细胞结构簇中。需要至少至少三个肺泡壁基底层堆积的细胞核,其宽度可达三个细胞。2)实性型:为实性片状的癌巣。3)复杂腺体。包括筛状结构、介于实性型和腺泡型之间的不良腺体、促纤维结缔组织增生中的融合腺体或不规则的带状腺体或小细胞簇或单细胞浸润。2021版WHO胸部肿瘤分类建议继续记录浸润性非粘液腺癌的组织学类型百分比,并利用这些特征用正式的分级系统(如下表)2.STAS:肿瘤气腔内播散定义为肿瘤细胞以微乳头、实性细胞簇、环状结构或单个癌细胞的形式离开原发灶,漂浮于肿瘤周围的正常肺泡腔内。出现了STAS的病例有较高的复发率,预后差。3.胸膜侵犯:胸膜分为脏层和壁层两部分,脏层胸膜被覆肺脏表面,并伸入肺叶间裂内,与肺紧密结合。壁层胸膜贴附于胸壁内面、膈肌上面和纵膈表面,脏层与壁层胸膜于肺根处相互移行,两者之间是一个密闭的胸膜腔。病理报告中PL0表示肿瘤位于胸膜下肺实质内没有胸膜侵犯;PL1表示肿瘤浸润突破弹力层;PL2表示肿瘤侵犯胸膜表面;PL3表示肿瘤侵犯胸膜壁层。弹力纤维特殊染色可以帮助病理医师判断有无胸膜侵犯。胸膜侵犯也是I期肺腺癌预后不佳的因素。4.脉管内癌栓:淋巴管或血管内有脉管癌栓也是早期肺腺癌术后复发和预后差的高危因素。治疗对于IA期肺腺癌患者不建议化疗,IB期需不需要化疗?美国NCCN指南推荐具有高危因素的患者“考虑”化疗,这个高危因素包括:低于45岁;病理提示低分化;病理提示脉管有癌栓;病理提示累及脏层胸膜;淋巴结检出数目过少;病理亚型为微乳头型。临床医生会结合病人自身因素选择治疗方式。
 郭俊红 主治医师 上海市肺科医院 病理科5583人已读
郭俊红 主治医师 上海市肺科医院 病理科5583人已读 - 精选 肺及胸膜疾病病理报告中常用免疫组化指标解读
免疫组化指标解读:(阳性用“+”表示,阴性用“-”表示)气管、肺、胸膜及纵膈疾病常用的免疫组化指标:1、TTF-1(甲状腺转录因子1):阳性部位:细胞核。主要用于肺肿瘤和甲状腺肿瘤的诊断。肺肿瘤中通常TTF-1(+)的肿瘤:肺腺癌、小细胞癌、硬化性肺细胞瘤。甲状腺肿瘤中,甲状腺滤泡性肿瘤、乳头状癌、低分化甲状腺癌和髓样癌TTF-1(+)。2、NapsinA:阳性部位:细胞质。主要表达于肺II型上皮和肺腺癌。通常与TTF-1联用,用于原发性肺腺癌与其他组织器官源性腺癌的鉴别。3、P40:阳性部位:细胞核。在肺鳞癌、淋巴上皮瘤样癌及胸腺瘤中P40(+)。4、CK5/6(细胞角蛋白5/6):阳性部位细胞质。常与P40联用诊断鳞癌、淋巴上皮瘤样癌。此外上皮样间皮瘤CK5/6+。5、CD56、Syn(Synaptophysin)、CgA(ChomograninA):三者联用,诊断神经内分泌肿瘤:小细胞癌、大细胞神经内分泌癌、类癌、不典型类癌。6、Ki67:阳性部位:细胞核。为细胞增殖标记,判断细胞增殖的程度。7、CK7:阳性部位:细胞质。在乳腺、肺等大多数上皮细胞中阳性,主要用于乳腺癌、肺癌与胃肠道腺癌的鉴别诊断。我们通常用CK7、CK20、CDX2、SATB2联用鉴别肺来源与胃肠道来源腺癌。8、CK:主要用于上皮源性肿瘤的诊断与鉴别诊断。9、ALK(D5F3):阳性部位:细胞质。用于检测ALK基因重排的方法之一,ALK激酶抑制剂,即克唑替尼的出现,对ALK阳性的晚期非小细胞肺癌是一种有效的治疗方法,它可以明显改善患者的临床预后,体现在客观缓解率(objectiveresponserate,ORR)的提高,同时对延长无进展生存期和改善患者生活质量方面疗效显著。10、PD-1ligand,PD-L1(程序性死亡分子1(programmeddeath1,PD-1)/PD-1配体):信号通路的激活可导致免疫抑制性肿瘤微环境形成,使肿瘤细胞逃避机体免疫监视和杀伤,而阻断PD-1/PD-L1信号通路可以逆转肿瘤免疫微环境,增强内源性抗肿瘤免疫效应。目前免疫检查点阻滞剂抗PD-1、抗PD-L1抗体因其特异性强、副作用低、肿瘤控制时间长等优点已成为治疗非小细胞肺癌新方向,在临床实验中不断取得突破性进展。11、间皮瘤诊断常用指标:WT-1,CR,BAP1,CK5/6,D2-40,GATA3,CK,Vimentin,以上联合应用辅助诊断间皮瘤。
郭俊红 主治医师 上海市肺科医院 病理科5人已购买 - 精选 肺小结节(磨玻璃)之微浸润型腺癌
微浸润腺癌的定义:是指孤立而离散的小(≤3cm)腺癌,以贴壁生长方式为主,任何切面的浸润灶最大径始终小于5mm,常为非粘液型。判定浸润成分的标准为:出现贴壁以外的任何生长方式的成分(腺管、乳头、微乳头、实性、胶样胎儿型),或肿瘤细胞浸润到含有肌成纤维的间质中,或沿肺泡壁生长的肺泡腔内出现肿瘤细胞等均视为浸润。而当肿瘤浸润到淋巴管、血管或胸膜时即便是浸润成分最大径≤5mm时,要诊断为浸润性腺癌。微浸润性腺癌常常是在健康体检中进行胸部CT检查时发现的小而不纯的磨玻璃结节,由于微浸润腺癌是出于发展和变化中的一种状态,因此,影像学的随访观察是非常必要的。微浸润腺癌属于T1a(mi)期,如果完整切除则可望彻底治愈。
郭俊红 主治医师 上海市肺科医院 病理科13人已购买 - 精选 肺小结节(磨玻璃)之原位腺癌的病理诊断(二)
前面我们在原位腺癌(一)中展示了原位腺癌的CT和手术标本的照片,下面我来介绍病理诊断原位腺癌的标准,很多病人问我:“郭医生,手术医生术前跟我讲我的结节是增生,手术之后为什么是原位腺癌?”,目前,肿瘤诊断最可靠的手段仍然是组织病理诊断学,被称为肿瘤诊断的金标准(golden standard),病理医师被称为医师的医师(doctor’s doctor)。而原位腺癌的诊断标准如下:显微镜的低倍镜看结构,如图1.肺泡间隔增宽。显微镜放高倍看细胞,如图2.肿瘤细胞有异型(蓝色细胞核增大等),肿瘤细胞沿肺泡壁连续排列。我们知道, 肺内发生 原位腺癌后往往可持续较长一段时间结节没有变化,我们通过 CT 影像观察到的原位腺癌病例( 最长可达 10年) , 其手术切除后的病理证实肿瘤未发生浸润性改变。图1图2
郭俊红 主治医师 上海市肺科医院 病理科3565人已读 - 图文文章 肺实性结节一定是肺癌吗?肺部CT表现为实性结节的可能性疾病之一:从症状到诊断和治疗
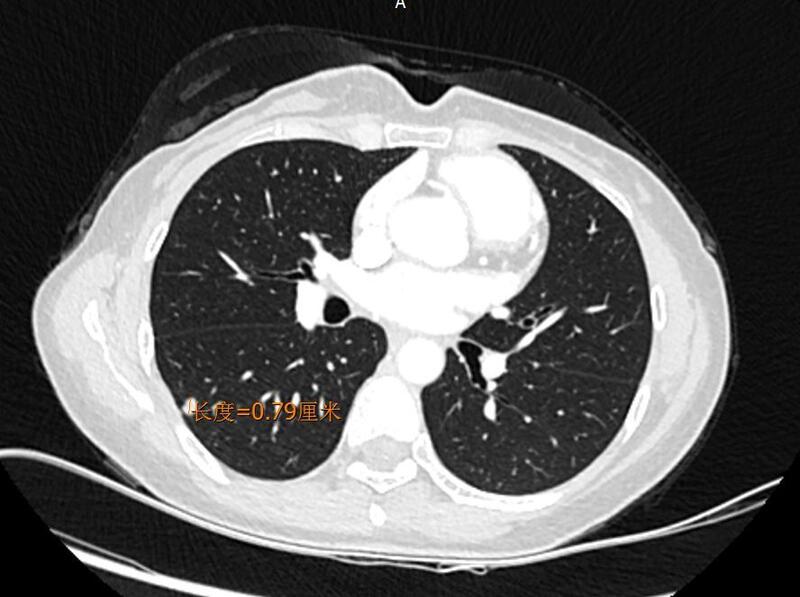
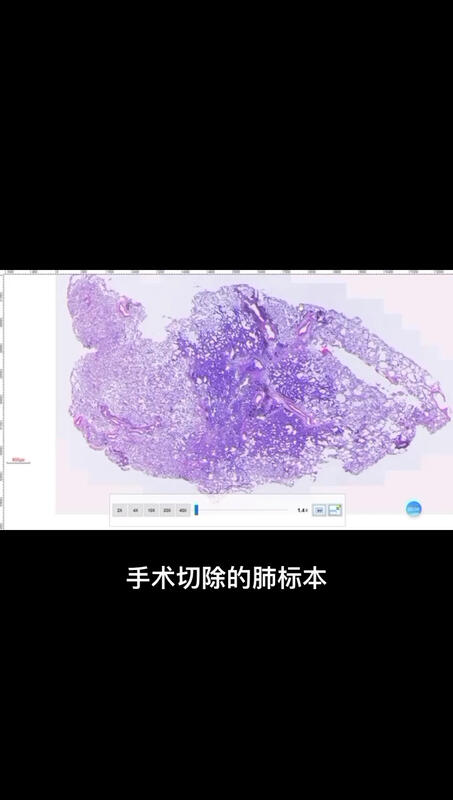
随着胸部高分辨CT和胸腔微创手术的推进,肺部小结节切除标本也更易获取,其中大部分为早期肺癌,也包括为数不少的非肿瘤性病灶。跟大家分享一种表现为肺部实性结节的病例。患者女,40岁,肺部高分辨薄层CT体检发现右肺下叶见一实性结节7.9mm,增强扫描有强化,肉芽肿性病变与恶性肿瘤难以鉴别,建议进一步检查。拿到CT报告的这位朋友,内心焦躁不安,吃饭睡觉都不香了,人到中年最怕意外和危机。人生如天气,可预料,但也常出乎意料。患者拿到CT报告诚惶诚恐的找到了胸外科医生,仔细阅读CT片后,单发结节病变病灶伴边缘毛刺,极易与肺部肿瘤相混淆,不能排除恶性可能,患者夜不能寐,茶饭不思,严重影响了生活和工作,胸外科医生建议其胸腔镜微创手术。由于CT表现为实性结节,良恶性不好判断,术中病理十分重要,术中病理良恶性直接影响术式,若为恶性要把整个肺叶切除;良性则只需切除小部分肺组织,从而保留更多的肺功能。 这个病例是我在工作中碰到的,结节是灰黄色的有光泽,有经验的病理医生会想到这有可能是个非肿瘤性病变,果然,术中病理报告:肉芽肿性病变,见可疑真菌孢子,考虑肺隐球菌病可能,待术后石蜡行特殊染色确诊。(术后石蜡病理:符合肺隐球菌病)。 生命的春夏秋冬,认识的起承转合,有时候真的令人难以琢磨,这位患者经历了过山车般的心情起伏,终于可以把一颗心放回肚里,是谁保住了她的肺?病理医生在此过程中起到十分重要的作用。肺隐球菌病是由新生隐球菌感染引起的一种亚急性或慢性深部真菌病,新型隐球菌是一种非遗传性、萌芽状的包裹酵母样真菌,存在于鸽子或禽类排泄物污染的土壤中,易形成气溶胶,人类常见的感染途径是呼吸道吸入,最常受累部位为中枢神经系统,其次为肺部及皮肤。肺隐球菌在明显免疫低下人群,尤其是HIV感染者中常见,但在一些有慢性基础疾病如高血压、糖尿病、器官移植或肿瘤患者及激素使用者,近年来发生于免疫正常的人群中检出率也不断增多。临床表现:常见的临床表现有咳嗽、咳痰、发热、胸痛,部分病例并无明显的临床症状,通常在临床体检中通过高分辨CT偶然被发现。肺隐球菌病影像表现缺乏特异性,病灶形态多样,可有单发结节、多发结节、斑片状,肺隐球菌病单发结节病变时,体积大小不一,病灶可伴分叶、边缘毛刺,极易与肺部肿瘤相混淆。血清CrAg检测快速无创,具有较高的敏感度及特异度。以8μg/L为截断值时,其特异度可达到100%。CrAg结果判读:荚膜多糖浓度<5.0μg/L,阴性;≥8μg/L,阳性;5.0~8.0μg/L,中介,应结合临床和影像综合评价。><5μg/L为阴性,≥8μg/L为阳性,介于5-8μg/L之间,应结合临床和影像综合评价。病理表现:组织表现与病期早晚而不同,早期表现为粘液瘤。晚期较常见,表现为肉芽肿性病变,在多核巨细胞内吞噬大量隐球菌菌体,隐球菌呈圆形、卵圆形,平均直径4-7μm,PAS和六胺银染色阳性,粘液卡红染色也可阳性。治疗:研究显示,对于临床确诊的肺隐球菌病患者应首先评估机体免疫状态及有无全身播散,再根据症状轻重程度分级治疗。对于非重症患者首选抗真菌药物治疗,推荐氟康唑200~400mg/d,疗程6~12个月。对于行手术完整病灶切除的患者,术后是否给予抗真菌治疗仍有争议。对于单发肺部病灶绝大多数病人手术后不需要治疗,极少数术后会复发。
 郭俊红 主治医师 上海市肺科医院 病理科2351人已读
郭俊红 主治医师 上海市肺科医院 病理科2351人已读 - 视频 肺结节之微浸润型腺癌病理诊断的详过程
 郭俊红 主治医师 上海市肺科医院 病理科929人已观看
郭俊红 主治医师 上海市肺科医院 病理科929人已观看 - 医学科普 非妇科细胞学报告解读
由于细针穿刺对病人的创伤小,方便、经济快速,是我院临床医生非常喜欢的检查手段,因此我院非妇科细胞学病例每年超8万例,包括常规涂片和液基涂片,积累了很多宝贵的制片及诊断经验,本科室细胞学标本种类也很丰富,包括以下几个种类: (1)支气管镜刷检; (2)CT或B超引导下细针穿刺; (3)浆膜腔积液; (4)支气管肺泡灌洗液; (5)EBUS-TBNA(超声内镜引导下经支气管针吸活检术) (6)痰细胞学; (7)细胞块包埋; (8)其他:小探头、磁导航等。非妇科细胞学报告有以下几种情况: 1、 标本无法诊断或不满意,应当结合临床及患者情况再取标本。 2、 良性病变:多为炎性病变、肉芽肿性病变(如结核、结节病等)、真菌感染等,这类一般不需要手术。 3、 意义不明确的非典型病变或可疑恶性肿瘤:如报告中提示异型细胞、疑恶性等,不能确定是否为恶性肿瘤,需要重取标本或结合临床随访后重取标本。 4、 恶性肿瘤: (1)明确恶性肿瘤,但不能分型,需要增加组织学活检,结合免疫组化诊断。 (2)明确恶性肿瘤,可以明确为非小细胞肺癌的,临床可根据患者情况手术或化疗,并可利用剩余的标本进行基因检测。 (3)明确肿瘤类型(如肺腺癌、鳞癌),临床可根据患者情况手术或精准化疗,并可利用剩余的标本进行基因检测。
郭俊红 主治医师 上海市肺科医院 病理科2647人已读 - 医学科普 常规石蜡病理报告解读
1、 大体描述: 病理医生需要对不同标本进行检查,包括小活检和不同大小的肺切除标本及更复杂标本,对肺标本的最基本的5个组成部分进行系统检查:气道、肺实质、浆膜、血管及淋巴结。大体描述主要包括以下几个内容:(1)手术方式及送检结构/器官标本大小。(2)是否有病灶,病灶大小及位置。(3)病灶的颜色、质地、边界。(4)病灶与支气管切缘或者肺切缘的距离。(5)病灶与大气道、浆膜、大血管的关系。(6)若有多个病灶,分别按照以上内容描述,并描述病灶之间的关系。(7)清扫的淋巴结的大小和个数。 2、 病理诊断: 病理诊断包括以下:(1)送检组织/器官名称(如左肺上叶);(2)肿瘤组织学类型及亚型(如角化型鳞癌);(3)是否浸润脏层胸膜、血管、神经。(4)手术切缘有无肿瘤;(5)淋巴结有无转移或其他病变如肉芽肿。
郭俊红 主治医师 上海市肺科医院 病理科7913人已读





